中和滴定の「あの曲線」の謎
みなさんこんにちは!
ともきです!
勉強は早い時期からやったもん勝ち!
「今すぐ」この記事を「最後まで」読むことで、
早い時期から勉強に「差」をつけよう!
本題へ移る前に軽く復習しよう。
化学基礎や化学で学んだ「中和滴定」
中和滴定で重要なのは、
水素イオン濃度([H+])なんだ。
これを表す代表的な指標として
pHがあるのも学校で学んだはずだ。
pHを数式で表すと、
pH=-log10[H+]
の形になるんだったね。
酸・塩基の滴下量を横軸に
pHを縦軸にして、
その関係を表現した曲線を
滴定曲線というんだ。
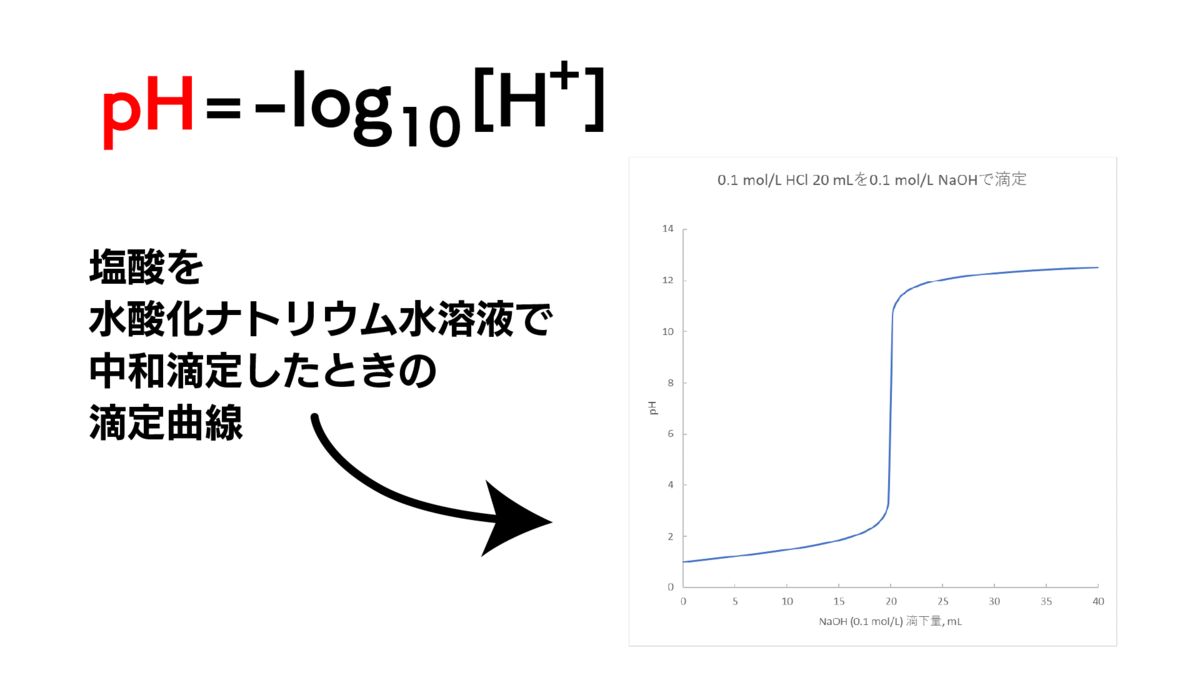
復習はここまでにして本題へ移ろう。
滴定曲線が水素イオンと水酸化物イオンが
同じ濃度になった中和点付近では、
pHが急激に変化している。
これをpHジャンプというが、
どうしてこれが起きるのか?
今回はこの謎を解き明かすよ!
塩酸を水酸化ナトリウム水溶液で
中和滴定する際の水素イオン濃度は
直線的に減少していく。

水素イオン濃度が0になる所が中和点。
しか~し!
実際は水素イオン濃度はゼロにならない!
水は、塩酸とは違って
"ほんの少しだけ"水素イオン([H+])と
水酸化物イオン([OH-])
に電離する化合物だ。
だからこそ、中和点を超えても
"ほんの少しだけ"水素イオンが
残ってしまうんだ!
純粋な水の電離では、
25℃で、[H+]=1.0×10^(-7) [mol/L]
だけ残ってしまう。

さて、pHとは対数関数であった。
水素イオンが0.1mol/Lに減るまでと
0.1mol/Lから10^(-7)mol/L
に減るまでに必要な
NaOHの滴定量をそれぞれ考えよう!
具体的な数値を求める必要はない。
大事なのは変化量!
前者よりも後者の方が
必要なNaOHが少ないのはグラフから明らか。
すなわち、少ない滴定量で
水素イオン濃度は
数桁分だけ一気に小さくなる!
非常に微量なNaOHで
桁が一気に小さくなるからこそ、
中和点付近でpHが急激に変化する!

これが
pHジャンプのメカニズム!
もしも説明が理解出来なかったら
このブログを何度も熟読したり、
数学の対数関数を復習して
完璧にマスターしよう!
本日はここまで!
一読ありがとうございました!