有機化合物は「丸暗記」で覚えちゃダメな理由!
みなさんこんにちは!
ともきです!
みなさんは、
有機化学で覚えるべき化合物が膨大で
暗記に挫折した…
という経験はありませんか?
僕も経験がありますし、
確かに高校化学で登場する有機化合物は
非常に多いです。
そこで、今回は具体的な化合物名ではなく
有機化合物の大まかなジャンル
を整理していこうと思います。
どうして「ジャンル」なのでしょうか?
化合物名を地道に暗記するよりも
ジャンル別に体系的に覚えた方が
覚えやすいからです。
例えば、ジエチルエーテル(CH3CH2OCH2CH3)
の構造式を覚えるとします。

エーテルという「ジャンル」に
属していることを知らなければ、
「一番左の炭素に水素三つついて、
その右の炭素に水素二つ、
その右に酸素原子が結合して…」
と非常に長ったらしい覚え方になります。
これでは不便ですよね。
逆にエーテル化合物なのを知っていれば
「エチル基が二つ挟んだエーテル」
とたった一言で覚えられるようになります。
化学に限らず、世界史などでも
語呂合わせの方が覚えやすいこと
一度は経験したことがありますよね?
それと全く同じなのです!
これからは無闇な丸暗記ではなくて
体系的に覚える癖を付けるように
実践してみてください!

そうすれば短い日数で成績が良くなります!
皆さんの将来に桜が咲き誇ることを
期待しています!
今回はここまで!
次回は具体的に有機化合物を
ジャンル分けしていきます。
一読ありがとうございました!
瞬殺!分子の立体構造を推定する3STEP
みなさんこんにちは!
ともきです!
今回は分子の立体構造を
簡単に推定できちゃう
方法を伝授しちゃいます!
分子の立体構造は
脳内でイメージしにくいですよね。
「二次元の絵なら想像できるけど、
三次元は限界(脳みそ爆発)…」
そんな人が多いと思います。

実際に、自分もそこで苦しんだ
経験があります。
脳みそオーバーフローする気持ちにも
納得できます。
しかし、適切な判別方法さえ知っていれば
たとえ三次元構造がイメージできなくても
簡単に判別することができます!
今回はそのための3STEPを
具体的にご紹介します!
Step1
まずは電子式を書く。

分子の形を推定するのに
電子式を使う発想は多くの人には
イメージしにくいと思います。
知っている分
他の受験生と「差」がつく
ということです!
電子対反発則を使って推定するので、
電子式を書く必要があるんだと
思ってください。
Step2
中心原子のまわりの電子対を数えて、
電子対の方向を定める。
電子式が書けたら中心電子の電子対を
数え上げましょう。
ここからが大事で、
その本数が分子の立体構造を
ほぼ決定するのです!
電子対は互いに反発しております。
すなわち、電子対同士の距離が
最も離れる位置に電子対が移動するのです。
(これをVSEPR則といいます)
中心原子の電子対が…
4本なら:正四面体
3本なら:正三角形
2本なら:直線
の形になるのです!
(ただし、非共有電子対が無い場合に
限られます)
STEP3
最後に原子核の位置を線で結べば
分子が完成します!
このように、無理にイメージするのではなく
条件分岐のプログラムみたいな
判別方法のほうが、
ずっと確実に推定できます!

ぜひ、この3STEPを覚えておいて
模試や定期考査などで
実践してみてください!
今回はここまで!
一読ありがとうございました!
僕が重宝した化学の参考書!?
みなさんこんにちは!
ともきです!
今回は自分が受験勉強で
重宝した「化学の」参考書について
お話しします!
参考書を読む時に
学ぶべきポイントが書かれていなくて
読みにくい場合がありますよね。
それによって、
無駄に時間を喰ってしまい
勉強効率がだだ下がりになります。

では、どうするべきか?
答えは簡単で
覚えるべき要点がまとまってる
参考書が手っ取り早いのです。
自分で一からノートにまとめる作業は
確かに覚えやすいのですが、
そのぶん時間がかかります。
参考書に目を通しただけで
内容が覚えることが出来れば
時間短縮はもちろんのこと
記憶力の向上につながります!

僕がオススメする参考書は
旺文社が出版している
化学 標準問題精講
というものです。
問題と解答冊子が別々になっていて
102のテーマに分けられた標問には
テーマ別に覚えるべきポイントが
凝縮しております。

迷ったら化学 標準問題精講
で演習してみてください!
今回はここまで!
一読ありがとうございました!
覚えなきゃ「ヤバイ」化学反応熱!
みなさんこんにちは!
ともきです!
化学の教科書の中盤辺りで
反応熱や格子エネルギーを学びます。
(自分が使った教研出版はそうだった)
熱のやり取りを数式で捉えるための
熱化学方程式に関して、
定義される反応熱は多種多様であります。
ヘスの法則を用いて
化学反応で発生する熱量を計算する際、
「各反応熱の定義を曖昧に覚える」と
符号ミスが起こり時間の無駄に
なってしまいます。

今回の記事では
反応熱の定義を整理します。
これらをノート等に書き留めておいて
覚える作業は今すぐに誰でも出来ます。
短期間で成績アップを狙いたい受験生
にはオススメの記事になります。
(1)化学反応にともなう熱
化学反応にともなう反応熱は
発熱反応は正の値、吸熱反応は負の値
になることに注意しておきましょう。
生成熱:
化合物1mol が成分元素の
単体から生成するときの熱量
燃焼熱:
物質1mol が完全燃焼するとき
に発生する熱量
燃焼熱は必ず発熱反応です。
溶解熱:
物質1mol が多量な水に
溶解するときの熱量
中和熱:
中和反応で1mol の水が生じるときに
発生する熱量
中和熱は必ず発熱反応です。
水和熱:
気体状のイオン1mol が多量な水中で
水和イオンになるときに発生する熱量
水和熱は必ず発熱反応です。
具体的な反応例を
写真に載せておきます。

(2)状態変化にともなう熱
状態変化にともなう反応熱では
絶対値のみで表すのが普通です。
(ただし、熱力学方程式では発熱は正、
吸熱は負になるように符号を書こう)
融解熱:
物質1mol が融解するときに
吸収する熱量(吸熱反応)
蒸発熱:
物質1mol が蒸発するときに
吸収する熱量(吸熱反応)
凝固熱:
物質1mol が凝固するときに
発生する熱量(発熱反応)
凝縮熱:
物質1mol が凝縮するときに
発生する熱量(発熱反応)
昇華熱:
物質1mol が昇華するときに
発生したり吸収する熱量
(発熱・吸熱反応の両方になりえる)

これら10個の反応式の定義を
数分・1時間の短時間ではなくて、
少しずつ覚えていってください。
遅くても一週間で全て暗記できます。
これを適切に暗記するだけで
反応熱の計算問題の正答率が
劇的に改善されます。
あれこれ熟考する前に、とにかく素早く
行動に起こすことが大事です。
本日はここまで!
一読ありがとうございました!
正しく教科書を使って成績に「革命」を起こそう!
みなさんこんにちは!
ともきです!
英単語を暗記するときに
どれだけ暗記しても
結果を出せないことはありませんか?
それは勉強効率が悪い証拠!
この記事では教科書に
ちょっとした工夫を加えることで
勉強効率を向上させる方法を
伝授しようと思います。
この方法は教科書さえあれば、
いつでもどこでも実践できます。

本記事は数分で読めるので
読まずにスルーするメリットは無く、
損しかありません。
時間をかけずに
模試の偏差値を上げたい!
そんな方におすすめな方法です。
STEP1
教科書全ページ眺めてみる
例えば英語の教科書があるならば、
一回は全ページ眺めてみましょう。

一言一句全て覚える必要はありません。
このとき重要なのは、
「どの分野が登場するか
大雑把に把握すること!」
例えば英語の教科書ならば、
「この会話表現が頻出だな」
「ある英単語を強調してるな」
など、些細なことで構いません。
たとえ習ってない範囲でも
教科書を一回読んだだけで
✓どこを学ぶべきなのか
✓どこを学ばなくても大丈夫か
を見極める能力が大事になります。
STEP2
覚えるべき部分をアウトプットする
箇条書きで構いません。
教科書から学ぶべき・覚えるべき部分を
ノートに書き出してみてください。

もちろん despite「~にもかかわらず」
のように英単語を列挙しても構いませんが、
「自分は○○が苦手だから、○○をすぐ覚える」
みたいに、
自分がすぐに実践すべきこと・しなくてよいこと
を書ければさらによし!
今すぐやるべきタスクが組めることで、
勉強時間を短縮することができます。
以上の手順を踏むことで、
勉強効率が高まって
成績向上する可能性が高まります。
最終的に受験を制するのは
自分の努力次第です。
今回はここまで!
一読ありがとうございました!
参考書は「必ず必要じゃない」理由
みなさんこんにちは!
ともきです!
今回の話は化学の話ではなく、
勉強のスタイルに関する話だ!
勉強のやり方&考え方を適切にすれば
勉強効率が改善して
短期間で得点アップが狙えるぞ!
これは誰もがすぐに実践できること。
「今すぐ」この記事を「最後まで」読むことで、
早い時期から勉強に「差」をつけよう!
大学受験は難しい問題が沢山。
特に二次試験では、受験生を選別するために
共通テストより問題がハイレベルに!
そこで大事になるのが参考書の存在。
教科書は誰でも理解できる入門書として
かなり初歩的な内容しか学習できない。
早慶・東大レベルまで対応できる参考書は
受験勉強にはうってつけなアイテム!

しかしながら、
✓自分に合う参考書が分からない
✓予算に合わせて購入するべき…?
そんな疑問が尽きない人が多い…
今回はこの疑問に着目するよ!
結論から言うと、
「先に全範囲復習してから
参考書選びを検討するべき!」
どうしてかというと、
あらかじめ全て復習することで
自分の苦手ポイントを抽出できるからだ!

例えば、理想気体の状態方程式で
正答率が著しく低くなったとする。
その分野が明らかに苦手ポイントだから、
「そこを重点的に学べる参考書を買うべき」
なのは容易に導けるよね!?
「とりあえずハイレベルだから」
という浅はかな理由で参考書を買っても
「内容が理解できずにお手上げ状態…」
と参考書代の無駄遣いに終わってしまう…
さらに、
解答ミスを恐れる完璧主義な人は要注意!
苦手ポイントと向き合わないことで
誤った勉強方法になるからだ!(僕の実体験)
自分は、
勉強が出来る人≠頭の良い人
と考えている。
僕が定義する「頭のいい人」は、
「ひらめき能力が高い人」の意味。
(すなわちIQが高い人)

例えば、高い塀をよじ登ろうとするとき
素手で登るのではなくて、
周りにある物体を土台にすれば
よじ登る難易度が大幅に低減される。
では、どうして
「土台を置けば簡単によじ登れる」
という考えに至ったのだろうか?
登山家やレスキュー隊員でもない限り
事前に「塀の登り方」を勉強しないし、
知識として意識的に
脳内に蓄えてたわけでもない。
まさに本能に近いようなもので、
それを適切な時と場合で偶然思いつくのが
ひらめき力だと僕は考えている。
一方、勉強が出来る人は真逆で
意識的に蓄えた知識を
いつでもどこでも思い出せる人をいうんだ!

さらに、勉強が出来る人は
論理的な思考力が十分備わってる!
例えば、参考書の購入を検討する場合に
最終目標を「第一志望校合格」なのに
✓デザインがかっこいいから
✓何となくハイレベルそうだから
で参考書選びをするとどうなるだろう?
参考書の目的:苦手ポイントを減らすこと
と
最終目標:第一志望校合格
の間に論理的なズレが生じてしまう。
そんな人は論理的に考えられないから
勉強効率が最悪になるのは
言うまでもないよね…(汗)
裏を返せば、論理的な思考力さえ備われば
勉強が出来る人と言えるわけだから、
勉強が出来る人≠必ずテストで満点取る人
の関係式も導かれるね!
さらに、この関係式からも
勉強に完璧主義を求める必要はないことが
連鎖的に分かるよね!?
この記事の内容をまとめると
✓まずは苦手ポイントを洗い出し
✓それを克服可能な参考書を購入するべし!
✓論理的な思考力が勉強出来る人
✓勉強に完璧主義はいらない
の4点が大事になってくる。
実は本記事を読むことで
論理的な思考力のチェックにもなるんだ。

点と点を線で結ぶように文章同士の関係が
全て理解できたならば、
論理的な思考力を持つ証拠になる!
本記事タイトルの意味も理解できるはずだ!
本日はここまで!
一読ありがとうございました!
銅の錯体ってどうして正方形なの?
みなさんこんにちは!
ともきです!
勉強は早い時期からやったもん勝ち!
「今すぐ」この記事を「最後まで」読むことで、
早い時期から勉強に「差」をつけよう!
さて以前の記事について、
錯イオンの立体構造には
配位子の数&VSEPR則
の二つが関わっていることを学んだ。
配位数:2個 ならば 直線形
配位数:4個 ならば 正四面体形
配位数:6個 ならば 正八面体形
になるんだったね!
しか~し! 例外が存在する!
テトラアンミン銅(II)イオン:[Cu(NH3)4]2+
テトラヒドロキシアルミン(III)酸イオン:[Al(OH)4]-
は配位子が4つしかないのに
正方形形になるんだ!

今回はこの「謎」を解き明かしていくよ。
銅イオンの「謎」
あらかじめ注意しておくと、
テトラアンミン銅(II)イオンでは
高校化学の範囲を大幅に超えた
大学で学ぶ高度な知識が必要なんだ。
今回は高校生でも理解できるように
かみ砕いて説明していくよ~
一言に要約して説明すると、ズバリ!
「本当は6配位の錯体なんだけど
ヤーンテラー効果で形が歪んで
正方形のように見える」

初めて聞く単語が登場したはずだ。
まず「ヤーンテラー効果」とは何だろうか?
ヤーンテラー効果とは、
「エネルギーを安定化しようとして
分子の立体構造が変化すること」
を意味する化学用語だ!
この場合は、
正四面体形や八面体形ではなくて、
正方形形がエネルギー的に安定である
ことがいえるね!
今度は配位数に着目してみよう。
水分子は極性分子であるから、
酸素原子は負に
水素原子は正に帯電している。

すなわちイオンに近い状態なので、
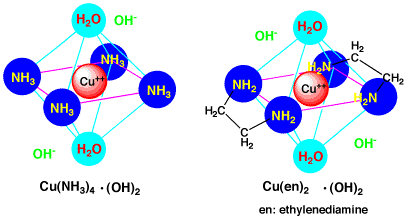
さらに水分子が二つ結合するのは容易で
実際は「[Cu(NH3)4(H2O)2]2+」
の6配位で存在している。
4配位ではなく6配位になる理由はこれだ。
これ以上の詳細な説明は、
d電子だったり、縮退の解消だったりと
高校では理解し難い概念が多数登場するので
省きます! すみません!
それではお粗末なブログになっちゃうので、
ヤーンテラー効果が起こりやすい錯体を
説明しておきます。
それはズバリ!
・遷移金属の八面体形錯体
・銅(II)錯体
が起こりやすくなる条件だ!
これをテトラアンミン銅(II)イオンに適用すると、
・本当は6配位になる
・銅(II)イオンが中心原子
と、見事条件に一致してる!
だからこそ、テトラアンミン銅(II)イオンは
✓ヤーンテラー効果を起こしたがって
✓正方形形になることで
✓エネルギー的に安定になるんだ!

正直、大学入試で問われない題材だけど
覚えておいて損はないし、
落単のリスクを少しでも回避できるなら
頭に留めておく程度に知っておくべき!
本日はここまで!
次回はテトラヒドロキシアルミン(III)酸イオン
の理由について説明するよ。
一読ありがとうございました!