「溶解度積」って何だっけ?
高校生の皆さんこんにちは!
受験勉強してますか?
化学を勉強してる皆さんは、
硫化物沈澱を覚えていますか?

実は!
硫化物沈澱の生成条件は
入試に頻出な部分!
そこを「何となく」のままにすると
大事な入試本番でつまずく
危険性大!
今回は、
硫化物沈澱が生成するpHを
整理していくよ!
これを理解するには始めに
「溶解度積」という考え方を
知らなければいけない。
溶解度積とは、簡単に言うと
溶液中の陽イオン
&陰イオンの積
のこと
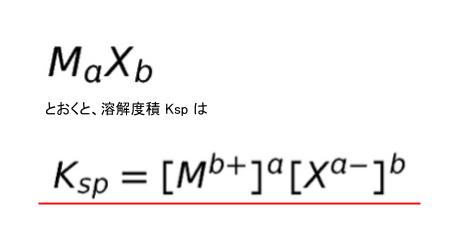
硫化水素を例に挙げると
水溶液中の電離反応は
H2S → H+ + S2-
すなわち [H+]^2[S2-] が
陽イオンと陰イオンの積になり
溶解度積となるわけだ
水素イオン&水酸化物イオンは
微量だから
細かく考える必要nothing!
また、溶け始める時の値をKspとすれば、
[H+]^2[S2-]>Ksp 沈澱ができる
[H+]^2[S2-]=Ksp 沈澱ができ始める
[H+]^2[S2-]<Ksp 沈澱ができない
関係が得られるのも覚えよう!
今回はここまで!
続きは次回のブログで!
一読ありがとうございました!